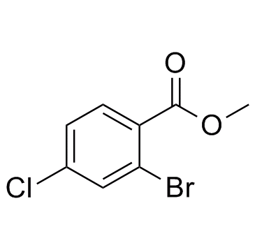
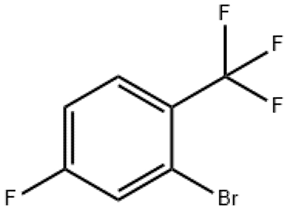
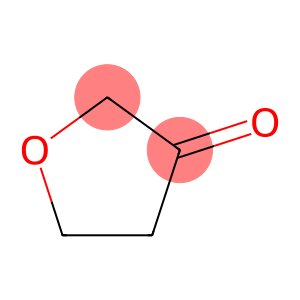
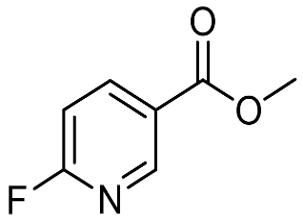
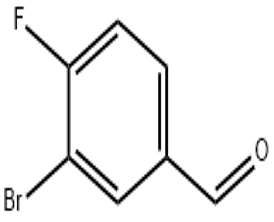
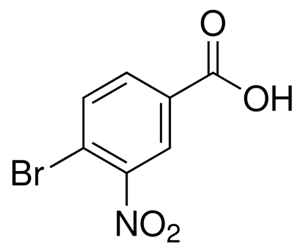
alpha-Ionone (CAS # 127-41-3)
| Risiko Coden | R42/43 - Kann Sensibiliséierung duerch Inhalatioun a Hautkontakt verursaachen. |
| Sécherheet Beschreiwung | S24/25 - Vermeiden Kontakt mat Haut an Aen. |
| WGK Däitschland | 2 |
| RTECS | EN 0525000 |
| TSCA | Jo |
| HS Code | 29142300 |
alpha-Ionon(CAS # 127-41-3) Informatiounen
Violett Keton, och bekannt als Benzophenone, ass eng organesch Verbindung. Hei sinn e puer Sécherheetsinformatiounen iwwer Ionone:
1. Toxizitéit: Violett Keton huet gewësse Toxizitéit fir de mënschleche Kierper. Et kann Schied un den Zentralnervensystem an der Liewer verursaachen, a kann negativ Auswierkungen op de Fortpflanzungssystem an Embryonen hunn.
2. Inhalatiounsgefor: D'Inhalatioun vum Damp oder de Stëbs vum Ionon kann Unbequem Symptomer wéi Schwindel, Schläimkeet, Husten a Schwieregkeeten verursaachen. Laangfristeg Belaaschtung kann Schied un den Zentralnervensystem verursaachen.
3. Kontakt Gefor: Violett Keton kann duerch d'Haut absorbéiert ginn. Laangfristeg oder extensiv Kontakt kann Haut- an Aenirritatiounen verursaachen. Entspriechend perséinlech Schutzausrüstung wéi Handschuesch a Sécherheetsbrille solle gedroe ginn beim Ëmgang mat Ionon.
4. Feierläschmoossnamen: Am Fall vu Leckage oder Feier, benotzt trockenem Pulver, Schaum oder Kuelendioxid fir de Feier ze läschen. Vermeit Waasser ze benotzen, well violett Keton mat Waasser reagéiert fir brennbar Gase ze produzéieren.
5. Offallentsuergung: Entsuergt Offall violett Keton richteg am Aklang mat lokal Reglementer a Regelen. Entlooss et net an d'Kanalisatioun oder Dreckskëscht.
6. Stockage Virsiichtsmoossnamen: Violett Keton soll an engem cool, dréchen, gutt gelëfter Plaz gespäichert ginn, ewech vun Quelle vu Feier an oxidants.
Dës Informatioun ass nëmme fir Referenz. Wann weider Notzung oder Veraarbechtung vum Ionone erfuerderlech ass, kuckt w.e.g. op déi zoustänneg Sécherheetsdatenblat a konsultéiert e Fachmann.
Natur
Violett Keton, och bekannt als Linaylketon, ass eng natierlech Ketonverbindung. Et ass den Haaptkomponent vum Aroma vu violett Blummen.
Violett Keton ass eng faarweg bis hellgiel ueleg Flëssegkeet déi liichtflüchteg ass bei Raumtemperatur.
Violett Keton ass löslech an Alkohol an Ether Léisungsmëttel, a liicht löslech am Waasser. Seng Dicht ass relativ niddereg, mat enger Dicht vun 0,87 g/cm³. Et ass empfindlech op Liicht a kann ultraviolet Strahlen absorbéieren.
Violett Keton kann zu Ketonalkoholen oder Säuren a chemesche Reaktiounen oxidéiert ginn, a kann op Alkohole reduzéiert ginn duerch Hydrogenéierungsreduktiounsreaktiounen. Et kann Alkyléierungs- an Esterifikatiounsreaktioune mat ville Verbindungen duerchgoen.
Applikatioun a Synthese Method
Violett Keton (och bekannt als purpurroude Keton) ass eng aromatesch Ketonverbindung. Et huet spezielle Geroch a gëtt dacks an der Parfum- a Parfumindustrie benotzt. Déi folgend ass eng Aféierung an d'Benotzung an d'Synthesemethoden vum Ionon:
Zweck:
Parfum a Gewierz: d'Dofteigenschaften vum Ionone, dee wäit an der Parfum- a Gewierzindustrie benotzt gëtt fir violett Parfumprodukter ze fabrizéieren.
Synthese Method:
D'Synthese vum Ionon gëtt allgemeng duerch déi folgend zwou Methoden erreecht:
Oxidatioun vum Nukleobenzen: Nukleobenzen (e Benzenring mat engem Methylsubstituent) gëtt un enger Oxidatiounsreaktioun ënnerworf, sou wéi eng oxidéierend Säure oder eng sauer Kaliumpermanganatléisung ze benotzen, fir Ionon ze generéieren.
Kopplung vu Pyrylbenzaldehyd: Pyrylbenzaldehyd (wéi Benzaldehyd mat Pyridinringsubstituenten an der Para oder Meta Positioun) gëtt mat Essiganhydrid an aner Reaktanten ënner alkalesche Bedéngungen reagéiert fir Ionon ze bilden.